独家解读:世卫公布进入三期临床的3种中国新冠疫苗是哪些?


独家抢先看
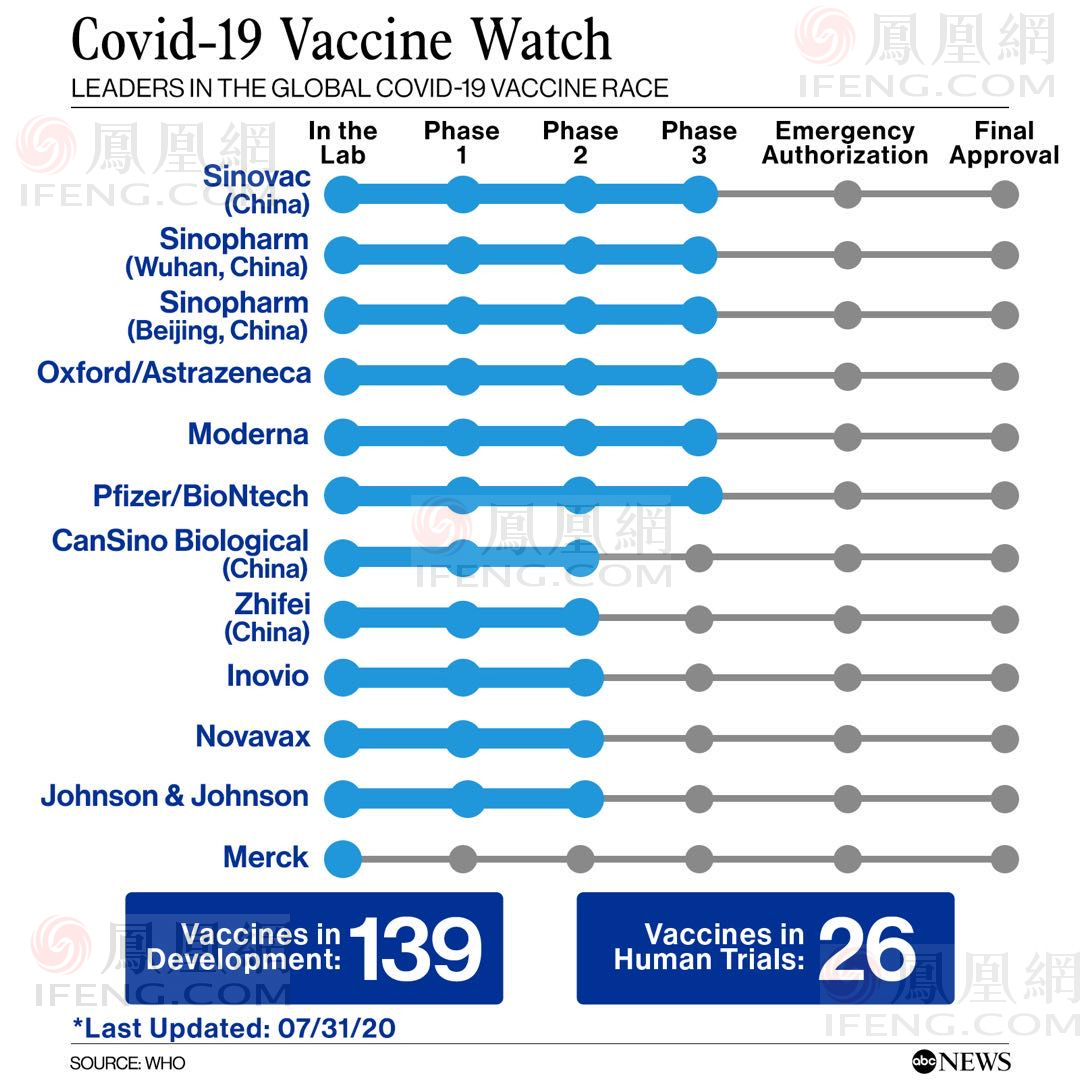
8月6日,世卫组织卫生紧急项目负责人迈克尔·瑞安表示,目前全球约有165种疫苗处于试验阶段,26种进入临床试验阶段,六种已处于三期临床试验阶段,其中三种来自中国。 据凤凰网肿瘤情报局了解,这三种是北京科兴中维的一款灭活疫苗及中国医药集团有限公司(简称:国药集团)的两款灭活疫苗,分别来自武汉生物制品研究所和北京生物制品研究所。还有三种是牛津大学/阿斯利康的腺病毒载体疫苗,美国莫德纳公司的mRNA 疫苗,辉瑞公司/德国BioNTech的 mRNA 疫苗。 陈薇院士/康诺希的腺病毒疫苗目前尚未正式进入3期临床。
相关阅读:陈薇院士疫苗三期试验未启,中国这款疫苗有望12月紧急上市?
文/张洪涛 宾夕法尼亚大学医学院 副教授
核心提要
1.康希诺公司/陈薇院士的人腺病毒载体疫苗Ad5-nCov,自7月20日发布了其第二阶段试验的结果后,到目前为止,尚未宣布有关第三阶段试验开始的信息。据悉其正与俄罗斯、巴西、智利和沙特阿拉伯等国就3期试验进行谈判,预期将在8月开展3期试验。
2. 目前中国的疫情基本消除,对于疫苗的临床试验是一个难事,因为不可能在一年或者数年之内完成研究。要开展3期临床试验,只有走出国门,到疫情比较严重的国家,例如科兴选择了全球确诊人数仅次于美国的巴西。
3. 美国辉瑞的疫苗已经定下目标,要在10月份之前完成三期试验及相关的评估报告,向FDA提交审批的申请,并在年底前将1亿剂疫苗交给川普政府。对于美国来说,今年是大选年,更为特殊,在11月投票选举总统之前,疫苗研发成功,将有重要的政治意义。
4. 科兴在巴西开展的3期临床试验的预期完成时间为2021年10月。虽然在今年年底前,科兴有希望看到效果,但是否能够长期有效需要等待时间的考验。科兴的临床试验设计,最终也是要比较注射疫苗后长达一年内的保护效果。
5. 面对菲律宾等友邦的需求,中国在提供帮助之前,首先应该让受助国对疫苗有充分的了解,能够仔细、周全地考虑疫苗可能出现的不良反应,不要对疫苗抱有不切实际的期望。中国也应该尽量通过符合国际规范的渠道来提供疫苗,避免给自己带来不必要的麻烦。
6. 不管是药物还是疫苗,都涉及到人命关天的问题,必须要经过严格的临床试验,完成对疗效和安全性的验证,才能正式批准使用。如果优先将市场定位为海关、航空、旅行服务、医疗服务等行业高风险人群,只要有一款疫苗获得成功,中国的疫苗供应就不会有问题。对于长时间没有出现疫情的当地人, 以及50岁以下的年轻人,新冠感染后的症状相对较轻,都可以谨慎一些,没有接种疫苗的迫切需求。
7.俄罗斯在2期临床之后直接批准疫苗,抢夺全球第一个批准疫苗的风头,但其实中国军方与石油公司海外员工、部分医疗系统员工近万人已施打康希诺的疫苗。从已有的数据看,新冠疫苗接种后会带来发烧、头疼、疲劳等一定程度的不适。
8. 目前确实也无法判断出到底哪个疫苗会成功,所以美国政府才采取大撒币的方式,广签合同,也是特朗普为谋求大选连任打的一张牌。相比之下,中国就比较讲人情,疫苗的临床试验还没有完成,不但参加试验国家的疫苗包下了,友邦国的请求也允许了。
中美各两款,英国一款疫苗,
陈薇院士疫苗暂未开展三期,其加拿大临床试验也再遇阻
7月27日,美国莫德纳公司(Moderna)和辉瑞公司(Pfizer)分别同时正式开始了新冠疫苗的三期临床试验,两家都是mRNA 疫苗,试验都是计划入组30000名自愿者。在这一天,两家的临床试验都开打了第一针。阿斯利康(AstraZeneca)的新冠疫苗三期临床已经在英国和巴西做了快一个月了,在美国的试验计划在8月开始。接下来展开三期临床实验的还有强生(9月)和Novavax(10月)。
在此之前,中国医药集团有限公司(Sinopharm,简称:国药集团)的灭活疫苗,已于7月初在阿联酋启动了3期临床试验, 该国卫生部长是第一位注射疫苗的志愿者,预计入组1.5万人。
图:阿联酋的合作方为G42健康服务。该机构的董事长兼代理副秘书长也参加了临床试验。
北京科兴中维(Sinovac Biotech)的灭活新冠病毒疫苗,也在巴西正式开始了3期临床试验。 7月13日,临床试验开始招募接种疫苗的志愿者,5天内有近百万人报名。科兴的疫苗于20日运抵巴西,第二天正式开始给自愿者接种。该试验研究负责人为巴西布坦坦研究所的Ricardo Palacios 博士,同时在18~59岁和60岁以上两个年龄段的人群中进行测试。
据独家消息,康希诺公司/陈薇院士的人腺病毒载体疫苗Ad5-nCov,自7月20日发布了其第二阶段试验的结果后,到目前为止,尚未宣布有关第三阶段试验开始的信息。据悉这家公司正在与俄罗斯、巴西、智利和沙特阿拉伯等国就3期试验进行谈判,预期将在8月开展3期试验。
7月31日, 虽还未进入三期临床的康西诺,被称为新冠疫苗第一股正式上市发行。同日,关于这家公司与加拿大合作进行的临床试验,再曝出至今尚未启动。这项于5月中达成的协议表明,加拿大卫生部加拿大疫苗学中心对康西诺的“候选疫苗”进行临床试验。但负责这项试验的科学家,达尔豪西大学教授斯科特·哈尔珀林(Scott Halperin)在当天称,他们至今仍没有如期展开临床试验,原因是这些用于试验的疫苗产品,尚未得到中国海关的批准,可以运往加拿大。
7月似乎是全球这几款有前景的疫苗扎堆进入三期临床的“黄金月”。但中美英疫苗进展,显然引发了激烈的国际竞争。 8月1日,俄罗斯卫生部长米哈伊尔·穆拉什科(Mikhail Murashko)表示,俄罗斯准备从10月开始大规模接种自主研发的新冠疫苗。如果这个“疫苗卫星”成真,那么俄罗斯将成全球首个全民疫苗接种大国。不但超美,更是赶中,走在了前列。但美国免疫学家福奇,却公开质疑中俄疫苗的安全性。他称,希望中俄的疫苗给任何人接种之前,应该先测试。并宣称,美国将不会采用中俄两国的疫苗。
目前进入3期临床的这几款疫苗,是如今研究进展最快的新冠疫苗。中国的两款疫苗,都是灭活疫苗,采用的是传统的技术路线,而美国、英国的疫苗,都是相对比较新的技术路线(核酸疫苗、腺病毒载体疫苗)。对于一开始拿不到病毒的研究团队来说,采用新的技术路线,可以根据病毒的基因序列来设计疫苗,能够大大节省开发时间。但是从中国灭活疫苗的操作来看,其实传统技术路线的进展也可以非常迅速。
3期临床试验,是最后一个阶段的关健试验。但临床试验并不是“走过场”,“走流程”,并不是只要表演一下,最后都能被批准。 2019年2月,美国的一款呼吸道合胞病毒疫苗(ResVax)的3期临床试验就宣布失败了。这种疫苗的接种对象是孕妇,目的是为了降低新生儿中的呼吸道合胞病毒感染。在此之前,一款给老年人使用的呼吸道合胞病毒疫苗,也同样在3期临床试验中失败。
所有的临床试验都有失败的可能,在没有看到试验结果之前,无法肯定判断出试验最终是否能够成功。
在早期的临床试验中,并不能真正看出疫苗是否有预防病毒感染的效果,一般只能检测出人体是否产生特异性抗体或免疫细胞,这虽然与疫苗的保护作用有关系,但并不是直接的保护证据。只有在3期临床中,通过数据明显表明感染率在接种疫苗的人群中出现了降低,疫苗才能获得成功。如果不能证明一个疫苗有预防感染的效果,就没有接种它的必要。
疫苗安全性方面的问题也需要考虑。即便能顺利通过1期和2期临床试验,因为试验人数太少,也只能表明疫苗没有明显、严重的不良反应,并不能充分表明安全性没有问题。对于一款疫苗,需要对获益和风险进行综合评估,只有获益足够大,风险也可以承担,这款疫苗才值得推广使用。
所有这些安全性和疗效的数据,都来自于3期临床试验。
疫苗试验为什么会“肥水流入外人田”?
从3期临床试验的开展来看,大家也注意到了一个问题:中国的新冠疫苗3期临床试验,都跑到外国去做了。目前已公开参加试验的有加拿大、阿联酋、巴西、俄罗斯、智利和沙特阿拉伯等六个国家。
有人觉得,这是“肥水流到了外人田”。为什么中国自己研发的疫苗,不能先满足一下自己的需求呢?
要解释这个问题,必须再次提一下3期临床试验的主要目的:证明疫苗是否能有效防止感染病毒。
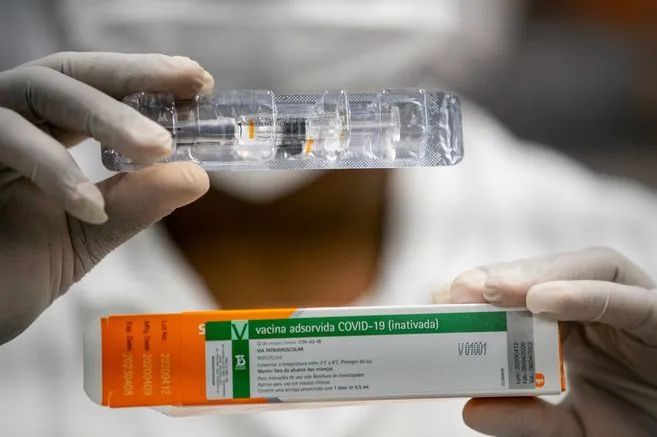
里卡多·帕拉西奥斯(Ricardo Palacios)医生,是巴西Butantan研究所的临床研究主任。他负责科兴Sinovac Biotech开发的冠状病毒疫苗的三期临床试验,有9000名志愿者于7月24号开始打第一针疫苗。
科兴公司在巴西使用的疫苗
巴西全球第二高发新冠病毒人数,使其成为了全球几个重要的疫苗三期临床的“全球实验室”。据称有将近六款疫苗在这里展开了竞赛。
疫苗的临床试验,与动物试验的操作完全不一样,不能把自愿者当小白鼠对待,在接种疫苗之后故意让受试者去接触病毒。所以,临床试验所测试的是在正常的生活状态下感染病毒的概率,试验的对照组表现的就是在没有疫苗情况下的感染率,而疫苗组则希望出现明显降低的感染率。
如果我们在国内做3期临床,会出现一个什么样的情况呢?
7月23日,根据国家卫健委的数据,中国新增确诊病例68例,其中本土病例为64例。以中国14亿人口来计算,感染比例为每亿人每天出现5个感染。
假设疫苗临床试验入组1万人,需要2000天才有可能出现一个感染!2000天,已经是5年多了!临床试验要比较出疫苗的效果,需要积累一定的感染病例,这就意味着需要几十年的时间才能完成!
面对着全球大流行的传染病,在自己的田地里慢慢做几十年的临床试验,这样的情况能接受吗?
有人觉得不能这么算,因为国内的疫情主要是在局部地区,如目前的新疆。确实,新疆只有2100万人口,在7月27日报道了70例确诊及无症状感染,感染比例为每百万人每天出现3例,这比全国的平均数高了60倍,能大大缩短试验时间,相当于是从4G提高到了5G,但这种局部爆发的感染率并不会持久,就像北京新发地爆发的疫情,在一个月内就消失了。所以,即便选择国内的疫情爆发点进行疫苗的临床试验,也不可能在一年或者数年之内完成研究。
可见,目前中国的疫情基本消除了,这本是一个好事,但是对于疫苗的临床试验来说,却变成了一个难事。
要开展3期临床试验,只有走出国门,到疫情比较严重的国家 。 科兴选择了巴西,这是目前确诊人数第二多的国家,仅次于美国,而且疫情严重到连巴西总统都被感染了。除了国药集团选择了阿联酋,康希诺公司/陈薇院士的人腺病毒载体疫苗Ad5-nCov,目前正在与俄罗斯、巴西、智利和沙特阿拉伯等国就3期试验进行谈判,预期将在近期开展3期试验。
国药集团疫苗阿联酋试验有难度,
康希诺公司/陈薇院士疫苗尚未启动,
科兴疫苗3期临床试验10月完成,成惟一可能在12月上市疫苗?
3期临床试验的开始比较重要,但是何时能够完成,更为重要,也是大家所迫切关心的问题。
美国辉瑞的疫苗,是与德国生物科技公司BioNTech合作研发的RNA疫苗。辉瑞公司已经定下了目标,要在10月份之前完成三期试验及相关的评估报告,向FDA提交审批的申请,并在年底前将1亿剂疫苗交给川普政府。为什么要抢在10月份之前呢?10月之后是秋冬,本来就是流感季,如果流感再与新冠混搭起来,伤害力就更厉害,所以如果在10月份能获得疫苗有效的准信,大家都会安心一点。对于美国来说,今年是大选年,更为特殊,在11月投票选举总统之前,疫苗研发成功,将有重要的政治意义。
值得一提的是,中国的上海复星医药也与BioNTech公司签署了合作协议,获得了德国BioNTech公司疫苗在中国的商业授权,目前正在开展早期临床试验。如果辉瑞的临床试验显示出疫苗的效果,可以加速此款疫苗在中国的审批。
总的说来,辉瑞的这个进度安排是惊人的,但是还有更惊人的!根据CNN7月29日的报道,俄罗斯计划在两周内批准一款新冠疫苗!俄罗斯的这款疫苗,至今尚未完成2期临床,按照预期,要在8月3日才能完成2期临床,看来战斗民族准备在2期结束后直接批准了。这样的事情,本来是难以想象的,但是今年在见证了新冠之后,感觉什么都有可能发生!战斗民族心里可能也有个小九九,如果这个疫苗搞不定新冠,再加一瓶伏特加就可以搞定。
中国研发的新冠疫苗什么时候能完成临床试验呢?在临床研究的正式登记网站上(clinicaltrials.gov),可以查到科兴在巴西开展的3期临床试验的预期完成时间为2021年10月。显然明年10月太久了,吃瓜群众关心的是今年10月能不能看出疫苗的效果。
巴西有两亿左右人口,7月29日确诊数为7万人,感染率为每万人中每天有3.5人感染。科兴的3期试验计划入组8870人,如果巴西能保持目前感染率,参加临床试验的志愿者在不打疫苗的情况下,平均每天会有3人被感染,在大约3个月的时间,会有300个人左右感染。因为试验有对照组和疫苗组,每个组又要分为两个年龄段,那么每一个小组本该会有70~80 名感染者。如果科兴的灭活疫苗有预防感染的效果,并且保护率能达到50%以上,那么通过这3个月所积累的感染数据,可以显示出明显的保护效果,试验也就有成功的可能性。
所以,在今年年底前,科兴是有希望看到效果的,而一但效果明确,相信中国会及时批准该疫苗。
关于在阿联酋开展临床的灭活疫苗,国药集团董事长刘敬桢曾在中央电视台表示,研究将会在三个月左右完成。据称,这位董事长与国药的近1,000名员工同时注射了疫苗,参加了这一试验。但如果仔细分析一下阿联酋的感染率,则会发现按时完成的困难比较大。阿联酋人口有一千万左右,如今每天的新增确诊在300例左右。国药集团的临床试验计划入组1.5万人,3个月累计才会有45人左右被感染。只有精准找到感染风险比较高的人群开展临床,国药集团才有机会在年底前看到疫苗的效果。
需要指出的是,即便试验在3个月内看到效果,也只能表明疫苗在短期内有保护作用。是否能够长期有效?这需要等待时间的考验。科兴的临床试验设计,最终也是要比较注射疫苗后长达一年内的保护效果。
当然,只要短期内保护效果明显,疫苗就有价值,即便长期效果不行,也只需要多次免疫接种而已。
由于对疫苗的认识有偏差,吃瓜群众对疫苗还抱着有一针见效的期望。一针见效固然比两针见效好,但是这并不是决定一个疫苗是否有效的关键。这就好比相亲谈恋爱,不能一见面就定一个“婚后生二胎”的目标。到底疫苗要打几针?还得根据临床试验的数据。
巴西沙特等参试国家将优先获得疫苗使用权?
中国能否满足友邦的疫苗需求?中国公司需谨慎预防各种疫苗供给风险
中国因为3期临床需要到国外开展,必然要与当地有所协议,在试验成功之后提供一些必要的疫苗及技术。据媒体报道, 在巴西开展3期临床的科兴公司,同意在试验成功之后,给巴西提供6千万人份的疫苗。同时,科兴也签署了技术转让协议,可以在当地建设生产线,自行生产疫苗。
同时,也有友邦国家在寻求中国的帮助,希望在疫苗成功之后能获得一些货源。7月27日,菲律宾总统杜特尔特发表国情咨文时表示,希望中国新冠病毒疫苗研发成功后优先向菲方提供。对此,中国外交部发言人汪文斌在28日的例行记者会上表示,“新冠肺炎疫情发生以来,中菲双方同舟共济、守望相助,抗疫合作已成为两国关系的新亮点。菲律宾是中国的友好邻邦,我们愿在疫苗方面优先考虑菲方需求。”
中国外交部应该会答应菲律宾的要求。7月27日,在中国、阿富汗、巴基斯坦、尼泊尔四国外长举行的应对新冠肺炎疫情的视频会议中,国务委员兼外长王毅主提出了四点倡议,其中第三点就是“增进抗疫与疫苗合作”。目前不清楚具体的执行方案。
需要提醒的是,面对友邦的需求,中国在提供帮助之前,首先应该让受助国对疫苗有充分的了解,能够仔细、周全地考虑疫苗可能出现的不良反应,不要对疫苗抱有不切实际的期望。中国也应该尽量通过符合国际规范的渠道来提供疫苗,避免给自己带来不必要的麻烦。
对友邦进行力所能及的帮助,相信大家都不会有异议,尤其对于传染病来说,只要疫情在一个国家不结束,就有传播扩散的风险,殃及鱼池,因此帮助别人也是帮助自己。但问题是,中国疫苗的产量到底会有多少?能否优先满足自己的需求?
根据目前的资料,科兴灭活疫苗的年产能为1亿剂。国药集团在北京生物制品研究所的新冠肺炎灭活疫苗生产车间,有1.2亿剂的年产能,同时在武汉生物制品研究还有1亿剂的产能。这些车间都是刚建成不久,到了年底前,如果疫苗都获得了批准,最多也只有2亿剂左右的存货,不可能让每一个人都打上疫苗。
但是,是否人人都需要马上去接种疫苗呢?
疾控中心主任高福为何可以提前施打疫苗,是特权还是临床试验?
国内这部分人群可能会优先获得“疫苗权利”?
7月26日,在一场网络研讨会中,中国疾病预防控制中心主任高福表示,自己已经注射了一种新冠疫苗,希望它能奏效。目前公开此事,高福是因为感觉到了反疫苗的情绪,希望能够建立大家对疫苗的信心。
疾控中心的工作其实也是很难做的,既怕公众拒接疫苗,又怕公众一窝蜂挤兑疫苗。不过现在最主要的矛盾,应该是供求不足的矛盾。试想一下,面对着前所未有的疫情威胁,经过正规临床试验的疫苗,还会可能不香吗?
有时候,某个政治人物或者科学家,为了表现出对某个疫苗的信心,会带头打疫苗。但是,不管这个人的政治影响力多大,这个科学家有多优秀,如果参加了临床试验,他们就跟其他的任何人没有本质的区别,只能提供一个数据点。从一个单一的数据点,无法推断出整个试验的结果。
不管是药物还是疫苗,都涉及到人命关天的问题,必须要经过严格的临床试验,完成对疗效和安全性的验证,才能正式批准使用。这与一般商品、保健品不一样,不是找一个网红来带货,就可以开始热销。
所以,如果把疫苗的市场定位为14亿国人,中国目前的产能肯定是远远不够的。但是,如果优先将市场定位为高风险人群,只要有一款疫苗获得成功,中国的疫苗供应就不会有问题。
哪些是高风险人群呢?中国目前面对的主要是输入风险,所以海关、航空、旅行服务、医疗服务等行业,都有较高的风险。 疾控中心人员如果需要到医院及疫情爆发地区进行调查,也必然属于高风险人群。相反,在信息透明的状况下,如果一个地区长时间并没有出现疫情, 生活在当地的人就没有接种疫苗的迫切需求。对于年轻人,比如50岁以下者,新冠感染后的症状本来也相对较轻,也没有接种疫苗的迫切需求。
对于没有迫切需求的人,完全可以谨慎一些,等等看。假设疫苗有某种小概率的严重不良反应,由于临床试验人数有限,这种小概率事件是不能在临床研究中充分暴露出来的,需要等疫苗上市之后,在推广过程中,才能逐步显现。
军方与石油公司海外员工、部分医疗系统员工近万人已施打疫苗?
疫苗接种一个多月效果如何?有何副作用?
即便目前未知疫苗是否会有小概率的严重不良反应,从已有的数据看,新冠疫苗接种后会带来一定程度的不适。
目前康希诺的人腺病毒载体疫苗,已经于6月25日被中央军委后勤保障部卫生局批准为“特殊需要药剂”,相信已经在军队内部中开始接种,尤其是边境地区以及疫情高发地区的军队人员,是一种应付紧急情况措施,所以有一年的有效期,并不能以此作为疫苗有效和安全的佐证。根据陈薇团队发表于国际医学期刊《柳叶刀》的早期临床研究结果,在接种此款疫苗的人中(低剂量,一针),有56%在注射部位出现疼痛,有16%出现发烧,28%出现头疼,44%出现疲劳。当然,这些副作用大部分都是轻微的,只有1%的人出现了3级以上不良反应 [1]。如果未来的临床试验能确认疫苗的保护性,那这些副作用的风险也就是可以承受的;反之,如果保护性尚不明确,只有在万不得已的情况下,面对着很高的感染风险,才应该考虑接种疫苗。
陈薇院士
国药集团的灭活疫苗,也已提供给一些国企的出国人员自愿使用。据媒体报道,中石油员工可以在海外工作时自愿选择使用两种“用于紧急情况”的疫苗中的一种来保护自己。但此说法并没有得到中石油公司的回应。
由于目前国外一些地方的疫情比较严重,对于为了工作必须到疫区的人员来说,尚未完成临床试验的新冠疫苗,也是一种选项,相当于参加了一个非正式的临床试验。目前有公开报道的除了上述疫苗的使用情况外,一些医疗部门的官员,疫苗研究部门的高管,包括疫情期间的前线医护人员,外交人员等,都在自愿的情况下,打了疫苗。客观地说,这部分人应纳入三期临床试验的一部分。如果有关部门能够正确地随访使用的情况,也可以在某种程度上帮助对疫苗效价及安全性进行评估。当然,这些自愿者也需要对疫苗效价和安全性的不确定性有充分的了解。
康希诺生物股份公司研制的候选疫苗是第一个进入二期测试的疫苗。这家总部位于天津的制药公司于7月31日上市,成为中国第一疫苗股。
前面提到战斗民族在2期临床之后直接批准疫苗,抢夺全球第一个批准疫苗的风头,但是真要比这个的话,康希诺的疫苗其实才是第一个批准,虽然只是限于军用。如果说到民用,国药集团的灭活疫苗实质上已经走在前面了。
总体来说,只要大家不要一窝蜂扎堆打疫苗,如果国内没有再次爆发大规模的疫情,只是有小规模、零星的疫情发生,国内对疫苗的实际需求其实并不巨大。 假设疫苗通过了3期临床试验,作为基建狂人的中国,也可以在短期内建成新的疫苗生产车间。比如说目前全球最大的疫苗生产车间,是国药集团在北京的车间,年产量为1.2亿剂,修建仅仅耗时60天。
不管是搞清楚副作用还是扩大生产,所有问题的关键点,是需要尽快通过3期临床试验。
科兴生物科技有限公司在北京的实验室
美国政府开巨额空头支票全球抢疫苗,设立疫苗防疫“美国壁㕖”?
美国虽然疫情控制很糟糕,但这个状况却给疫苗的临床试验提供了最优的条件,不用担心感染病例不够。也许因为这个原因,如今尚未开始3期临床的辉瑞,才有底气立下了在年底前完成申报,并提交疫苗给美国政府的目标。
冲着辉瑞的信心, 美国政府已经出资19.5亿美元,向辉瑞订购1亿剂疫苗,足够供5000万人使用(每人需要注射两次疫苗)。美国政府也不只是向辉瑞大撒币,之前也向莫德纳公司签署了9.39亿美元的协议,同时还向英国的阿斯利康公司支付12亿美元,预计订购3亿剂疫苗。不过请注意,目前这些疫苗公司还没有赚到美国政府购买疫苗的钱,最后能否赚到,需要看临床试验是否成功。不管怎样,通过这些商业协议,美国政府预计可以获得足够的疫苗,给美国国民接种。
正是因为形势所迫,美国政府对疫苗确实是一个开放的心态。7月21日,在被问及是否会与中国合作为美国民众研制疫苗时,美国总统川普说,“我们愿意与任何能带给我们好结果的人合作。”
当然,目前确实也无法判断出到底哪个疫苗会成功,所以美国政府才采取大撒币的方式,广签合同。
到底疫苗在大选前能不能成功,美国总统心里也没底,所以在7月30日,川普在推特上发文问大家:是不是该推迟选举呢?
美国的这个操作,与中国的表现又是天地之别。美国总统川普目前的口号是“美国优先”(America first!),从购买疫苗中也能看出。相比之下,中国就比较讲人情,疫苗的临床试验还没有完成,不但参加试验国家的疫苗包下了,友邦国的请求也允许了。
这也没有办法,谁让目前美国的新冠确诊数和死亡数都是世界第一呢。America first, 美国做到了。
有的第一,没有必要去抢。有的事情,能帮就帮!毕竟大家都要活下去。
参考文献:
1.Zhu, F.C., et al., Immunogenicity and safety of a recombinant adenovirus type-5-vectored COVID-19 vaccine in healthy adults aged 18 years or older: a randomised, double-blind, placebo-controlled, phase 2 trial. Lancet, 2020.